測定方法
ここでは、糖度・硝酸態窒素・酸度・糖酸比・果汁量・カロテノイド・ライマン価の測定について、
それらの測定方法を解説していきます。

液状の試料が必要です。
サトイモや長芋などの粘り気が強い品目でも、
擦り下ろした状態の試料で、
計測できる場合もあります。

スプーンの裏などで押して搾ることで、
試料が集められます。
葉物類やブロッコリーの蕾などの、
液状の試料を集めにくい品目は、
写真のように乳鉢ですりつぶしたあと、
搾るかフィルターで濾します。

滴下します。
STARTボタンを押すと、
糖度が表示されます。
そのまま同様の試料で計測できます。
その後、余分な試料をふき取り、
50秒間乾かします。
試験紙を挿入します。
10秒後に結果が表示されます。
ここでHIと表示される場合は、
硝酸態窒素濃度が高く、
原液試料のままでは計測できないので、
精製水で希釈して、
もう一度『 2.』 から行います。

そのまま同様の試料で計測できます。
糖酸度計ですので、
糖度・酸度同時に計測できます。

ビーカーに果汁1gを滴下し、
精製水で希釈します。
希釈倍率
ミカンなどの低酸度柑橘 ➡ 50倍
レモンなどの高酸度柑橘 ➡ 100倍

果汁をセンサー部分に滴下し、
STARTボタンを押すと、
糖度が表示されます。

今度は『2.』で作成した試液を滴下します。
STARTボタンを押すと、
糖度の下に酸度が表示されます。

Rのボタンを押すと、糖酸比がわかります。
検体を半分に切り、重さを量っておきます。
果汁の重さを量ります。
搾汁した果汁の重さを比較し、
果実の重さのうち、
果汁が何%を占めるのか算出します。

3g量り取ります。

ビーカーに半量ずつほど入れ、
試料3gと均質化(ホモジナイズ)します。

メスフラスコに移して混和させます。
その後、12本のチューブに入れます。
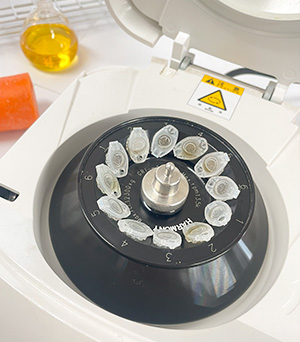
15,000rpmで5分間遠心します。
(1分間に15,000回転)


定められた4つの波長における、
吸光度を計測します。
下記の計算式を用いて、
計測した吸光度からカロテノイド濃度を
算出します。
ニンジンのカロテノイド計算式
β-カロテンの濃度 (mg/ℓ) = -1.292A443 + 3.698A492 + 0.131
総カロテノイドの濃度 (mg/ℓ) = 4.143A475 - 0.561
α-カロテンの濃度 (mg/ℓ) = 0.984A443 + 3.091A475 - 2.758A492 - 0.299
(ただし、A443 、A475 、A492 、は、それぞれ 443nm、475nm、492nmの吸光度)
金時人参については、
別の計算式を適用します。

1g量り取ります。

それぞれメスシリンダーで量り、
試料1gと均質化(ホモジナイズ)します。

メスフラスコに移して混和させます。

4本のガラスセルへ入れます。
この際、残滓が入らないよう注意します。

定められた4つの波長における、
吸光度を計測します。
下記の計算式を用いて、
計測した吸光度からカロテノイド濃度を
算出します。
とまとのカロテノイド計算式
クロロフィルaの濃度 (mg/100ml) = 0.999A663 - 0.0989A645
クロロフィルbの濃度 (mg/100ml) = -0.328A663 + 1.77A645
リコペンの濃度 (mg/100ml) = -0.0458A663 + 0.204A645 + 0.372A505 - 0.0806A453
β-カロテンの濃度 (mg/100ml) = 0.216A663 - 1.22A645 - 0.304A505 + 0.452A453
(ただし、A663 、A645 、A505 、A453 は、それぞれ 663nm、645nm、505nm、453nmの吸光度)
溶かす量は、
ライマン価ごとに決まっています。
測定するジャガイモのライマン価を
ある程度予測して、始めに溶かす
食塩の量を決めます。
ゆっくりと入れます。
浮いてきたら、その比重から、
ライマン価がわかります。
浮かなかった場合は、食塩を増やして
浮くまで繰り返します。
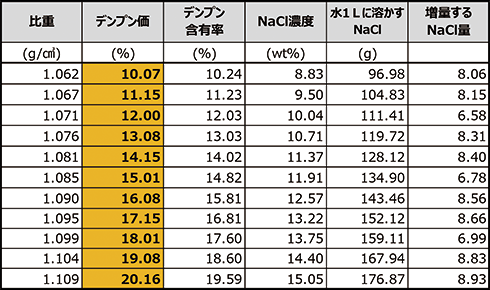
例えば 水1000mlに食塩119.72gを溶かし、
そこで検体が浮いてこなければ、
更に8.40gの食塩を追加で溶かします。
そこで浮いてきたならば、
その検体のライマン価は13ということになります。
そのため最初から浮かないように、
予測したライマン価より低い値の食塩量から始めます。
copyright(c) 2003-2026 Alphar Co.,Ltd.